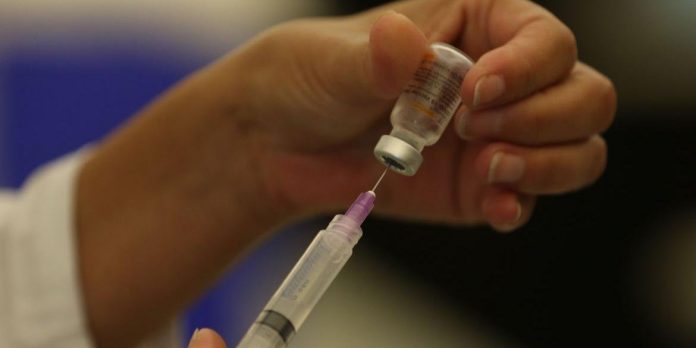
Pelo menos duas vacinas contra a Covid-19 que passaram pela fase de testes em hospitais de Porto Alegre, no ano passado, seguem esperando a aprovação da Agência Nacional de Vigilância Sanitária (Anvisa). Dezenas de voluntários gaúchos se submeteram aos estudos científicos dos laboratórios da chinesa Clover Biopharmaceuticals, no Hospital de Clínicas de Porto Alegre (HCPA), e da canadense Medicago/GSK, no Hospital Moinhos de Vento, que se iniciaram em meados de 2021. O problema para os voluntários, contudo, é ainda não poderem receber a carteira de vacinação, ou usar o aplicativo Conecte SUS para comprovar a imunidade.
Nesses estudos, os participantes voluntários recebem o imunizante ou um placebo, sem saber qual receberam, ficando meses sob observação dos médicos responsáveis, que conferem a reação do sistema imunológico à vacina. Nos estudos da Clover e da Medicago, os participantes não podiam receber outras vacinas disponíveis pelo SUS. Com isso, alguns desistiram do estudo para receber uma das vacinas disponíveis no Programa Nacional de Imunizações (PNI).
Os que permaneceram até o momento não tiveram a vacinação recebida no estudo reconhecida pelo SUS. “A comprovação de que se imunizaram, nós mesmos fornecemos”, explica Eduardo Sprinz, infectologista responsável pelo estudo da Clover no HCPA. O hospital oferece aos voluntários um ofício comprovando a participação no estudo, entretanto, eles não recebem carteira de vacinação, nem podem usar o aplicativo Conecte SUS. Mesmo assim, de acordo com o Sprinz, a validade é a mesma em relação a documentos oficiais do governo, permitindo, inclusive, viagens para fora do país.
A vacina da Clover teve os resultados apresentados pela farmacêutica em um artigo de setembro de 2021, demonstrando eficácia de 100% contra casos severos de Covid-19 e 84% em casos moderados a graves, causados por qualquer cepa do vírus. Além disso, não há efeitos adversos severos relacionados ao imunizante. Segundo Sprinz, esses resultados foram, ou serão, em breve, submetidos à Agência Europeia de Medicamentos, à Organização Mundial da Saúde (OMS) e à Anvisa. Mas a vacina ainda não conta com a aprovação do órgão brasileiro.
Apesar de parte do estudo ter sido realizado no HCPA, a responsável por buscar a aprovação e incorporação da vacina nos mercados nacionais e internacionais é a farmacêutica. Sobre o efeito desses vacinados, não reconhecidos pelo SUS, no vacinômetro, Sprinz explica que a quantidade de voluntários é muito baixa para que haja um impacto significativo.
Assim como o HCPA, o Moinhos não é responsável pela fabricação, composição ou aprovação da vacina da Medicago, tendo apenas coordenado parte da fase de testes da pesquisa. O resultado apresentados pelo imunizante da farmacêutica canadense apontou 71% de eficácia contra qualquer caso sintomático.
Mesmo com aprovação pelo departamento de saúde do governo do Canadá, a Covifenz acabou sendo rejeitada pela OMS. Isso ocorreu porque a empresa Medicago é ligada à multinacional de cigarros Phillip Morris, o que a entidade vê com receio.